Pólipo e Câncer Colorretal

Por Dr. Nelson de Souza Liboni
Compartilhe:
Pólipo
O pólipo colorretal é uma alteração causada pelo crescimento anormal da mucosa do intestino grosso (cólon e reto). Ele é uma projeção bem circunscrita acima do epitélio de superfície de mucosa, variando de 1 ou 2 mm a mais de 10 cm É uma das condições mais comuns que afeta o intestino, ocorrendo em 15 a 20% da população. Alguns são baixos e planos, outros são altos e se assemelham a um cogumelo, podendo aparecer em qualquer parte do intestino grosso (pediculado ou séssil). Inicialmente são diminutos e benignos (adenoma), podendo crescer até sofrerem transformação maligna (adenocarcinoma). Por este motivo é tão importante a remoção dos pólipos, com a finalidade de prevenir o câncer.
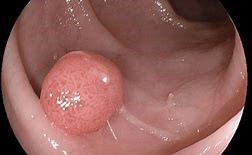
Podem ser hiperplásicos, hamartomatosos e adenomatosos.
Hiperplásicos
Eles são mais comum no reto, sigmoide, pregas de mucosa e válvulas de Houston. Notam se nas criptas revestimento de um epitélio hiperplásico. Não são neoplasias e não desenvolvem tumores malignos.
Hamartomas
Eles são de crescimento não neoplásico composta de uma mistura de tecidos anormais com tecido epitelial e conjuntivo. No cólon inclui pólipos juvenis e de Peutz- Jeghers. Existem diferenças entre polipose juvenil daqueles com pólipos juvenis solitários com um padrão autossômico hereditário e forte associação das neoplasias benignas e malignas do cólon e gastroduodenais com tratamentos diferentes.
Adenomas
Eles podem ser polipoides, vilosos e mistos. São benignos mas sua relação com desenvolvimento de câncer é importante.
- adenoma polipoide, pólipo adenomatoso, adenoma tubular -75% dos tumores benignos no cólon são classificados como adenomatosos e 10% vilosos. Podem ser pediculadas ou sésseis. Apresentam túbulos epiteliais agregados separados por lamina própria normal e crescem e ramificam horizontalmente a muscular da mucosa. Mitoses são observadas mas não há invasão da muscular da mucosa e podem ter displasias ou atípias.
- adenomas vilosos ou papiloma vilosos são frequentemente sesseis. Tem consistência macia e aveludada. Apresentam processos digitiformes cada um com cerne de lamina própria coberto por células epiteliais crescendo verticalmente na direção da luz intestinal.
- adenomas tubulovilosos, viloglandular, papilar, viloglandular, misto e adenoma polipoide viloso - são alterações intermediarias entre um viloso e polipoide.
Atenção a síndrome da polipose serrilhada é uma doença rara caracterizada pela presença de pólipos intestinais parecidos com os dentes de uma serra. Essa característica só pode ser identificada quando o pólipo é examinado sob o microscópio, por isso a colonoscopia é um exame fundamental para o diagnóstico da doença e remoção dos pólipos.
Pólipos intestinais surgem como resultado das alterações (mutações) dos cromossomos de algumas células da mucosa, fazendo com que modifiquem seu comportamento. As mutações podem surgir ao longo da vida. Por esse motivo foram realizados estudos que concluíram que a idade de maior risco para o surgimento dessas alterações (mutações) se inicia após os 50 anos. Entretanto, um maior risco de mutações pode ser transmitido dentro da família (hereditário), o que explica a importância de se pesquisar a história familiar.
Quando provocam sintomas, podem ocorrer sangramento, saída de muco com as fezes, alterações no funcionamento do intestino e, em casos raros, dores abdominais. Mas, na maioria das vezes não apresentam sintomas, sendo descobertos com maior frequência através de exames como a colonoscopia ou raios-X contrastados.
Os pólipos podem ser diagnosticados através de exames endoscópicos ou radiológicos. Três exames endoscópicos podem ser utilizados com esta finalidade: a retossigmoidoscopia rígida e flexível e a colonoscopia. A retossigmoidoscopia rígida permite a avaliação de aproximadamente 20 cm finais do intestino, enquanto a retossigmoidoscopia flexível permite o exame de 30 a 60 cm. A colonoscopia permite a avaliação de todo o intestino grosso. No exame radiológico chamado enema baritado (clister opaco) é injetado um contraste por via retal que irá mostrar as paredes intestinais no exame de raios-X e por ultimo colonoscopia virtual através da tomografia.
Exames mais simples também podem ser indicados para a detecção precoce. A pesquisa de sangue oculto nas fezes pode ser útil para selecionar pacientes candidatos aos exames completos como a colonoscopia. Mas, é importante enfatizar que um teste negativo não exclui a presença de um pólipo. A descoberta de um pólipo intestinal em um exame de retossigmoidoscopia obriga a uma completa avaliação do intestino, uma vez que até 30% desses pacientes poderão ter outros pólipos.
Todos os pólipos encontrados no exame endoscópico devem ser totalmente removidos e enviados para análise do médico patologista (exame histopatológico). A imensa maioria dos pólipos é removida através da colonoscopia, exame que permite a utilização de instrumentos delicados e especiais. Contudo, a localização e as características de alguns pólipos podem exigir sua remoção através de cirurgia.
Apesar da possibilidade de complicações (sangramento e perfurações), sua baixa incidência não deixa dúvidas a respeito do benefício de se propor a colonoscopia e a polipectomia como estratégia na prevenção do câncer de intestino.
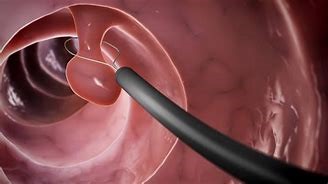
Uma vez que o pólipo é removido totalmente, sua recorrência (reaparecimento) não é comum. Podem surgir novos pólipos em locais diferentes, o que ocorre em cerca de 30% dos indivíduos.
O intervalo de tempo que um indivíduo deve voltar a realizar um exame depende dos achados do último exame, assim como do risco (pessoal e familiar) que cada indivíduo tem de desenvolver câncer intestinal. Algumas situações particulares caracterizam risco elevado para o câncer de intestino. Nestes casos a investigação através da colonoscopia é formal e o intervalo de tempo entre os exames deve ser abreviado, visando conferir proteção adequada.
Em suma, o surgimento dos pólipos pode estar relacionado a algumas síndromes e questões hereditárias. Estima-se que cerca de 40% das pessoas acima dos 50 anos apresentem pólipos colorretais: essas têm um risco 50% maior de desenvolver novas lesões após o primeiro diagnóstico.
Pessoas que sofrem com a Doença de Crohn e colite ulcerativa também estão mais expostas à formação de pólipos intestinais.
A adoção de uma alimentação saudável rica em fibras, frutas e verduras associada a atividade física é uma forma muito eficaz de diminuir os riscos não apenas de câncer colorretal.
Contudo, alguns dos principais fatores de risco são evitáveis, o que aumenta as chances de se prevenir:
- Tabagismo
- Alcoolismo
- Obesidade
- Sedentarismo
- Alto consumo de embutidos , carne vermelha, baixa ingesta de fibras e vegetais
- Outros
Câncer Colorretal
Tem incidência maior países ocidentais, aumenta com a idade, maior sexta década sendo a 4ª causa de morte nas mulheres e quinta nos homens. Mais comum em ordem decrescente reto, sigmoide e descendente, ascendente e transverso
O adenocarcinoma é o tipo histológico mais comum (diferenciado e indiferenciado) seguido dos carcinoides, sarcomas , linfomas , melanomas que são mais raros.
Epidemiologia
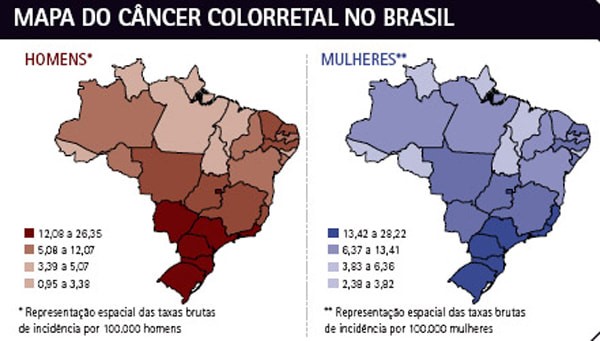
No mundo e no Brasil, o câncer colorretal é a terceira neoplasia maligna mais comumente diagnosticada e a quarta principal causa de morte por câncer.
O câncer colorretal é o terceiro mais frequente em homens e o segundo entre as mulheres no Sudeste. No Sudeste, esse número é cerca de duas vezes maior.
O perfil epidemiológico do Brasil e do mundo indica que a industrialização e o aumento da expectativa de vida são fatores determinantes para o aumento crescente no número de casos.
Apesar dos grandes avanços relacionados à genética, exames para diagnóstico e tratamento, o câncer colorretal é frequentemente diagnosticado em uma fase tardia, a partir do aparecimento dos sinais e sintomas como sangramento digestivo, alterações do habito intestinal e emagrecimento, quando a sobrevida em 5 anos é drasticamente reduzida para menos de 50%.
Mais de 90% dos cânceres colorretais são diagnosticados acima dos 45 anos de idade, população alvo para os exames de prevenção ou rastreamento.
Causas
Elas não estão totalmente esclarecidas. O mais aceito é que este resultaria da interação entre a predisposição genética e os fatores ambientais.
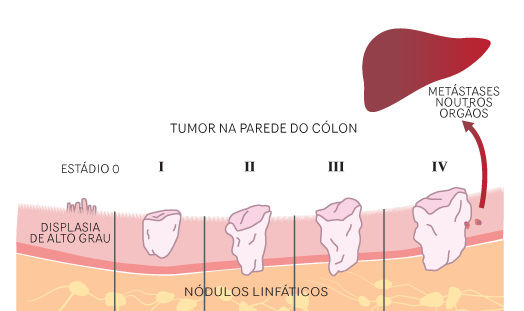
O câncer colorretal é uma neoplasia maligna que se origina no cólon, reto ou canal anal. A doença começa na camada superficial do revestimento intestinal (mucosa) e com o tempo vai atingindo as camadas mais profundas (submucosa, muscular e serosa) e outras estruturas adjacentes.
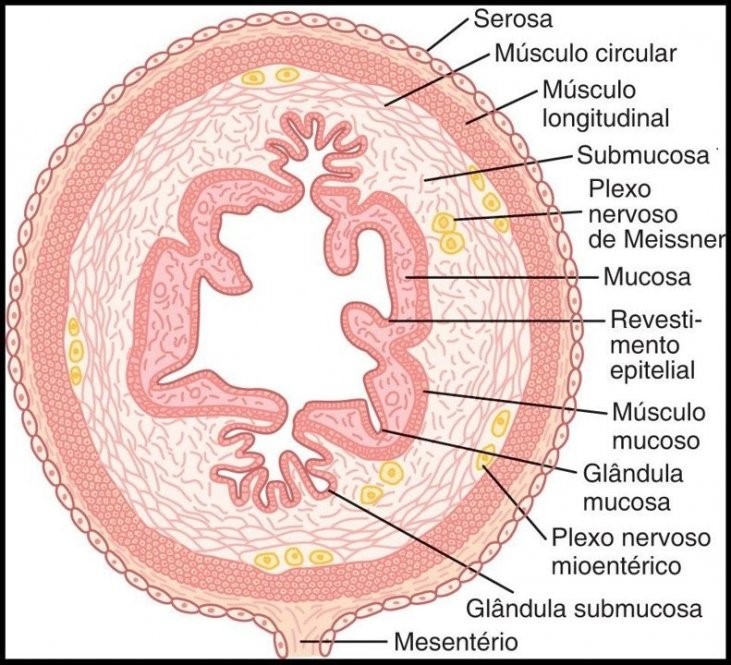
A presença de alterações genéticas predisponentes é indispensável e pode ser classificado em esporádico, familiar e hereditário.
É bem estabelecido que, em populações ocidentais e industrializados, a taxa de câncer colorretal é maior, assim como a migração de residentes em áreas de baixa incidência para as de alta.
Estima-se 5% a 10% dos cânceres colorretais estão associados alguma síndrome hereditária. Dentre os diversos aspectos que reforçam a importância do papel dos fatores ambientais no câncer colorretal está a constatação das diferenças regionais em sua prevalência e incidência.
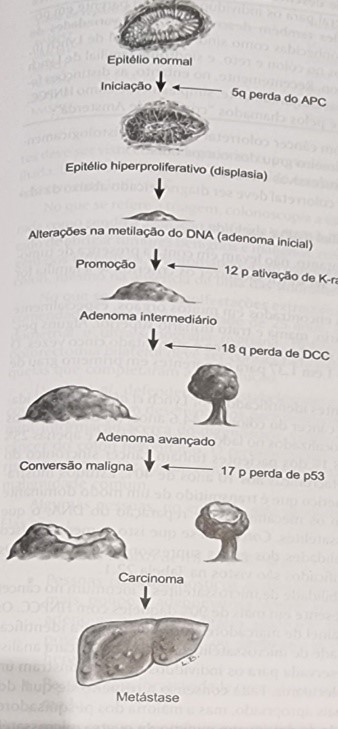
Presença de adenomas pela sequência transformação adenoma-carcinoma num acumulo de mutações distintas, sendo em casos esporádicos sem antecedentes familiares ou pacientes com síndromes polipoides (polipose adenomatosa familial nos colons, síndrome de Gardner quando acomete intestino delgado, ossos e adrenais, Turcot com tumores cerebrais todas com alteração no cromossomo 5).
O evento inicial ocorre na mutação do gene APC que leva a hiperproliferação epitelial. A seguir ativação da proteína K-rasque ativa crescimento e diferenciação das células epiteliais por estímulos extracelulares. Num terceiro momento, a mutação da proteína DCC associada as anteriores conduz a perda de aglutinação celular resultando num adenoma tardio e propicia metástases. No quarto momento a mutação da proteína 53 não detecta falhas no DNA e não impedem a divisão celular.
Os pólipos hiperplásicos não tem poder degenerativo, mas os adenomas vilosos, túbulo vilosos e tubulares participam na sequencia adenoma carcinoma, sendo portanto pre neoplásicos.
Nos pacientes com câncer coloretal hereditário não polipoide (HNPCC) ocorre a perda de função dos genes hMSH2 e hMLH1 que fazem o reparo celular no DNA entre outros. Estes pacientes tem historia de pelo menos portadores 3 parentes de 1º e 2º graus afetados, um deles com menos de 50 anos.
Outros aparecem de adenomas planos com coloração avermelhada e com alto potencial para neoplasia(serrilhados - SSA) é uma neoplasia do intestino grosso que pode evoluir para câncer colorretal. .Ela são lesões espraiadas ou lesões de crescimento lateral tipo LST são definidas por lesões superficiais do cólon maiores que 10mm e potencialmente invasão submucosa maior quando comparada a lesões elevadas. Não necessariamente são tumores malignos e aparecem em 10% pólipos colonicos .
Pelo protocolo de Kyoto podem ser granulares e não granulares que se dividem em planos ou pseudodeprimidos com maior chance de invasão. Os tumores a eles associados quando malignizam representam 20 a 30% dos canceres colorretais.
Esse tipo de crescimento também é conhecido como pólipo. É um crescimento plano, em vez de uma protusão das paredes do cólon, com células anormais que se estendem para a parede do intestino. O tumor pode ter uma forma serrilhada distinta e às vezes parece mimetizar dobras da mucosa normal no cólon.
A preocupação com um adenoma serrilhado séssil é que o tumor pode se tornar canceroso. Os pesquisadores identificaram um caminho que esses crescimentos podem usar para fazer a transição de crescimento excessivo benigno para malignidade e, embora isso não ocorra em todos os casos, ter um histórico de pólipos é um motivo de preocupação.
Fatores de Risco
I - Predisposição genética
Câncer esporádico
Quando a pessoa com o câncer colorretal é o único na família, não existe outros casos. Representa a maioria dos casos de câncer colorretal. O risco na população geral acima dos 50 anos é de que 1 pessoa a cada 500 desenvolverá o câncer colorretal.
Câncer familiar
Quanto mais pessoas de uma mesma família têm câncer colorretal, maior o risco de outro membro dessa família desenvolver o câncer colorretal. Alguém com parente próximo (pai, mãe, irmão, tios ou avós) com câncer colorretal, o risco para a doença aumenta muito, especialmente se a doença acometeu um parente com menos de 40 anos de idade. Nesses casos, todos os parentes devem fazer a colonoscopia de prevenção.
Quando já existe um parente de primeiro grau com câncer colorretal, mas não preenche os critérios para o câncer colorretal hereditário.
A relação é simples: Quanto mais membros da família são acometidos e quanto mais cedo a idade de diagnóstico, maior o seu risco.
Exemplos:
- - Se você tem um irmão ou pai que foi diagnosticado com câncer de cólon, o seu próprio risco de desenvolver câncer colorretal é de cerca de 1,7 vezes maior do que se você não tenha histórico familiar.
- - Se você tiver dois membros da família de primeiro grau com câncer colorretal, o risco é 2,7 vezes maior do que se você não tinha membros da família com câncer colorretal.
- - O risco é ainda maior se os familiares foram diagnosticados com câncer de cólon em uma idade com menos de 60 anos.
Câncer hereditário
Síndromes genética onde é alto o risco da ocorrência do câncer colorretal.
- - Polipose Adenomatosa Familiar - FAP, quando 100% dos pacientes desenvolverão o câncer colorretal até os 40 anos se não submetidos à cirurgia para retirada de todo o cólon e reto. Pessoas com FAP têm 50% de chance de passar a condição para o seu filho. As crianças que não herdam a condição de seu pai não poderão passá-la para seus filhos.
Cerca de um terço das pessoas com FAP não tem um dos pais acometido, portanto, tem uma mutação espontânea e podem passar FAP para os seus filhos com transmissão autossômica dominante. - - Câncer Colorretal Hereditário Sem Polipose - HNPCC = "Hereditary Nonpoliposis Colorectal Cancer" Síndrome de Lynch (SL) com riscos acumulativos maiores para o câncer colorretal (78%) e câncer do endométrio (43%), seguido pelo trato biliar, estômago, vias urinárias e ovário (19-9%). Apresentam ainda, um risco aumentado de tumores extra-cólicos (TEC), principalmente carcinomas do endométrio, ovário, estômago, intestino delgado, urotélio,pâncreas e vias biliares. Para os outros tipos de HNPCC, provavelmente relacionadas com o câncer, tais como intestino delgado e cérebro, o risco é apenas 1%. Ocorre geralmente em idades mais jovens, os tumores localizam-se principalmente no cólon direito.
Também conhecido como Síndrome de Lynch, a HNPCC é uma doença autossômica dominante responsável por cerca de 5% a 10% do total dos cânceres colorretais. É a síndrome hereditária mais comum de predisposição ao câncer colorretal.
Ainda que os critérios para diagnóstico de Amsterdam e tratamento estejam estabelecidos, o conhecimento da síndrome pela classe médica é insuficiente. Se comporta como na FAP, isto é, têm 50% de chance de passar a condição para o seu filho. Independe da atuação de fatores ambientais.
Critérios de Amsterdam usados para o diagnóstico da síndrome familiar
Pelo menos três casos de câncer colorretal (CCR), que preencham os seguintes critérios:- Um membro seja parente em 1º grau dos outros dois.
- Pelos menos 2 gerações sucessivas acometidas.
- Pelo menos um dos casos de câncer colorretal diagnosticado abaixo dos 50 anos.
- Polipose adenomatosa familiar deve ser excluída.
- Indivíduos com câncer colorretal com células em anel de sinete diagnosticado abaixo dos 45 anos.
- Indivíduos com adenomas diagnosticados antes dos 40 anos.
- Cânceres extra cólicos associados: endométrio, ovário, estômago, hepatobiliar, intestino delgado, células de transição da pelve renal ou ureter.
Os critérios de Amsterdam (CA), embora altamente específicos, têm valor muito limitado, inclusive para nossa população, pois são extremamente restritivos.
Assim, foram propostos os critérios de Bethesda, menos restritivos, com o intuito de levantar a suspeita de HNPCC e a utilização de testes laboratoriais, como a instabilidade de microssatélites, para auxiliar a definir um maior número de famílias de risco para HNPCC.
Critérios de Bethesda
- Indivíduos com câncer que preencham os critérios de Amsterdam.
- Indivíduos com 2 cânceres relacionados com HNPCC, incluindo câncer colorretal metacrônicos e sincrônicos ou cânceres extra cólicos associados.
- Indivíduos com câncer colorretal e um parente de 1º grau com câncer colorretal ou câncer extra cólico relacionado com HNPCC e/ou adenoma colorretal (um dos cânceres diagnosticado abaixo dos 45 anos e os adenomas abaixo dos 40 anos).
- Indivíduos com câncer colorretal ou endometrial diagnosticado abaixo dos 45 anos.
- Indivíduos com câncer de cólon direito com padrão histológico indiferenciado abaixo dos 45 anos.
Teste Genético para HNPCC
O diagnóstico de HNPCC pode ser realizado de duas maneiras: clinicamente, através do preenchimento dos critérios de Amsterdam; e geneticamente, pela identificação de mutações decorrente da instabilidade de microssatélites (MSI), fruto da inativação das proteínas de reparo do DNA. Mutações germinativas nos genes hMLH1 e hMSH2, dois dos principais genes do complexo MMR, estão presentes em 80% a 90% dos casos de HNPCC.
Embora isso pareça simples, na prática os médicos encontram enormes dificuldades para estabelecer tal diagnóstico, seja porque não dispõem de informações familiares adequadas com relação ao histórico do paciente, seja porque o sequenciamento genético não é ainda uma realidade na prática médica.
Protocolo de rastreamento de famílias em risco para HNPCC
Seleciona as famílias através dos critérios de Bethesda, seguido da investigação genética com a execução do teste de instabilidade de microssatélites (MSI) e/ou a imunohistoquímica para proteínas dos genes de reparo do DNA em amostras do câncer ressecado por cirurgia ou colonoscopia. Uma vez que um destes testes mostra-se alterado, passa para a pesquisa de mutações por sequenciamento nos genes de reparo do DNA.
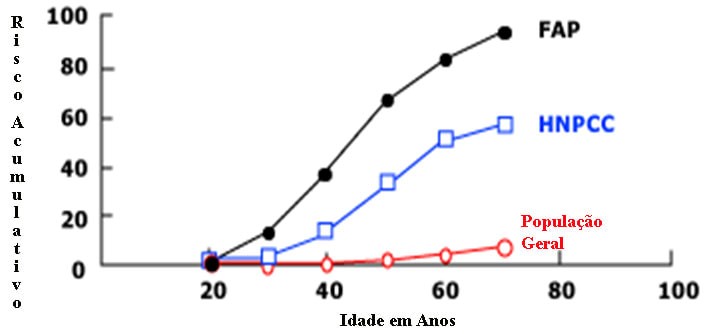
A tabela acima mostra o risco acumulativo do câncer colorretal levando em conta a idade e a presença ou não das síndromes hereditárias.
A diferenciação dos casos de HNPCC daqueles de câncer colorretal esporádico visa o aconselhamento genético, programas específicos de rastreamento e encaminhamento da família para análise mutacional no complexo MMR.
A ausência ou deficiência da função de reparo do DNA, mais precisamente a inativação das proteínas por alterações nos genes MMR, resulta em contrações ou expansões dos microssatélites (são sequências simples repetidas de DNA, que se repetem em tandem ao longo do genoma, formando sítios altamente polimórficos, o que possibilita o seu uso como marcas moleculares). Essa condição é chamada de Instabilidade de Microssatélites. Ela apresenta em 90% dos HNPCC diferente do câncer cólon retal esporádico.
O exame de mutações nos genes de reparo de DNA MMR (MLH1 e MSH2) na linhagem germinativa está indicado em tumores com instabilidade de microssatélites ou indivíduos pertencentes a famílias com HNPCC.
II - História pessoal de pólipos neoplásicos (adenoma ou serrilhado)
Aumenta o risco de câncer colorretal no futuro. O número e os tipos dos pólipos orientam o intervalo apropriado para a vigilância. Se houver incerteza sobre a história pessoal do pólipo e os registros não puderem ser obtidos, deve-se considerar que pólipo era neoplásico. O risco relativo varia de aproximadamente 3,5 a 6,5 em tais pacientes.
III - Radiação prévia
Uma história de radioterapia para câncer de próstata está associada a um risco aumentado de câncer retal. A magnitude do risco é aproximadamente semelhante à observada em pacientes com história familiar de adenomas do cólon.
IV - Flora intestinal alterada
Isso ocorre pela inflamação crônica da parede intestinal e mais susceptível a substancias oncogênicas.
V - Doença inflamatória intestinal
A retocolite ulcerativa e a doença de Crohn são doenças inflamatórias benignas que causam inflamação em graus variados na mucosa do intestino grosso. A doença inflamatória intestinal está associada ao maior risco de câncer colorretal, especialmente as com mais de 8 anos de tratamento que comprometem mais de 1/3 do intestino.
Existe maior risco nessa população com aumento de 10% a cada década para RCui e no Crohn numa média 15 vezes da população em geral pela inflamação crônica da parede intestinal e mais susceptível a substancias oncogênicas.
VI - Dietéticos
É bastante provável que certos alimentos e bebidas contribuam com o aparecimento dos pólipos intestinais, especialmente o consumo frequente e em excesso de álcool, carnes vermelhas ou processadas.
Especula-se, também, que o uso de conservantes químicos e excesso de alimentos gordurosos possam contribuir com o aparecimento. Entendem-se que o processamento e conservação das carnes com sal e conservantes, em especial os nitratos e hidrocarbonetos aromáticos policíclicos, que alteram a estrutura do DNA da mucosa, são elementos cancerígenos.
Com cautela, especula-se que o consumo diário de mais de 50g desses produtos aumentariam em 18% o risco de câncer colorretal.
A baixa ingesta de fibras vegetais pois elas aumentam o bolo fecal, diluindo os agentes carcinogênicos fecais e reduzindo o contato direto desses agentes com a mucosa intestinal, além de acelerar o transito.
Gorduras animais aumentam a degradação dos sais biliares pela flora bacteriana em compostos potencialmente tóxicos.
A baixa ingesta de cálcio (liga a ácidos graxos e sais biliares convertendo em composto cálcio insolúveis), vitaminas C e E, selênio ( como antioxidantes).
Os alimentos ricos em vitaminas A, C e E são a cenoura, batata-doce, abóbora, espinafre, brócolis, vegetais folhosos verdes escuros, germe de trigo, girassol, soja, ovo, abacate, frutas cítricas (laranja, limão), morango, kiwi, mamão papaia, acerola, pimentas vermelhas e couve-de-bruxelas.
O consumo de carne processada (salsicha, linguiça, bacon e presunto) é fator de risco certo e carnes vermelhas (carne de boi, porco, cordeiro, vitela, carneiro, cavalo e cabra), de um modo geral, são fatores de risco "provável".
A recomendação é que seja ingerida até duas vezes na semana, podendo ser substituída, nos outros dias, pelas carnes brancas, ovos e outras combinações de alimentos com valor proteico semelhante, como arroz com feijão.
VII - Bebidas alcoólicas
Elas associam o aumento no risco para câncer colorretal quando a quantidade ingerida de bebidas alcoólicas é moderada ou pesada, isto é, superior a 30 gramas de etanol por dia, cerca de duas doses de bebida destilada (75 ml), 2,5 taças de vinho (250 ml) e 3 copos de cerveja (1000 ml).
VIII - Tabaco
O tabagismo, inclusive os fumantes passivos, é fator de risco. É associado a maior incidência e mortalidade. Tanto para a incidência quanto para a mortalidade, a associação é mais forte para o câncer do reto do que para o câncer do cólon.
O tabagismo também é um fator de risco para todos os tipos de pólipos do cólon e reto. Para os pólipos adenomatosos, o risco é particularmente alto para adenomas mais avançados (isto é, ≥ 10 mm e para os com displasia de alto grau). O tabagismo também é um fator de risco para pólipos serrilhados do cólon.
IX - Baixo nível socioeconômico
Ele está associado a um risco aumentado de aproximadamente 30% quando comparado aos outros níveis socioeconômicos com inatividade física, dieta não saudável, tabagismo, obesidade e taxas mais baixas de rastreamento. Todas as pessoas devem refletir sobre seu estilo de vida e buscar equilíbrio dentro de suas possibilidades.
X - Obesidade
Avaliada pela relação cintura-quadril, está associada ao aumento no risco para o câncer colorretal.
XI - Idade
Ela é um importante fator de risco. O câncer colorretal é incomum antes dos 40 anos; a incidência começa a aumentar significativamente entre as idades de 40 e 50 anos. Quanto maior a idade, maior o risco.
Registros ocidentais sugerem que a frequência do câncer colorretal está aumentando no grupo abaixo de 45 anos, enquanto está diminuindo em grupos mais velhos. Decorre da maior aderência aos exames de prevenção do câncer colorretal nos pacientes acima dos 45 anos.
A literatura atual sugere que mais de 86% dos pacientes diagnosticados com menos de 50 anos são sintomáticos no momento do diagnóstico e, apesar disso, apresentam um estágio mais avançado no diagnóstico e piores resultados.
Fatores protetores para o câncer colorretal
Um grande número de fatores protetores é descrito em estudos como associados a um risco menor de câncer colorretal.
I - Atividade física
Dados sugerem que a atividade física regular, seja ocupacional ou de lazer, está associada à proteção do câncer colorretal. Redução significativa de até 25% no risco de câncer colorretal quando comparado com os indivíduos menos ativos. O mecanismo subjacente à aparente associação protetora de atividade física não é conhecido.
II - Dieta
- Frutas e vegetais
Muitos estudos epidemiológicos mostraram a ação protetora da dieta rica em frutas e vegetais. Dados sugerem que pode haver pouco benefício em aumentar o consumo de frutas e vegetais além dos níveis associados à ingestão de uma dieta razoavelmente equilibrada. Em comparação com os não-vegetarianos, os padrões alimentares vegetarianos também são associados a um risco significativamente reduzido de câncer colorretal.
- Fibras
Vários estudos laboratoriais, nutricionais e epidemiológicos identificaram um papel para a fibra alimentar no desenvolvimento do câncer colorretal. No entanto, o grau em que a fibra dietética protege contra o desenvolvimento do adenoma/serrilhado ou câncer colo é incerto.
O tipo de fibra pode ser um fator importante, como a ingestão de fibra de cereais não processada (insolúveis), que pode ser mais eficaz nos benefícios em comparação com formas mais processadas. - Ácido fólico
Não está claro se o ácido fólico tem papel na prevenção do câncer colorretal. Por outro lado, a possibilidade de que a suplementação de ácido fólico aumenta o risco de câncer de cólon também foi levantada. Dados observacionais sugerem que a suplementação com ácido fólico pode ser benéfica no estágio pré-adenoma, mas não além disso.
- Vitamina B6 (piridoxina)
Os dados disponíveis sugerem uma associação modesta entre maior consumo de vitamina B6 (piridoxina) e menor risco de câncer colorretal.
- Cálcio e produtos lácteos
Outro possível fator de proteção é o aumento da ingestão de cálcio suplementar ou dietético. Pelo menos três estudos controlados confirmaram a eficácia da suplementação de cálcio na prevenção da recorrência de adenomas colorretais, mas talvez não reduza o risco do câncer colorretal.
O efeito protetor do cálcio para adenomas convencionais depende da constituição genética de cada pessoa. A suplementação de cálcio tem sido recomendada para a prevenção primária ou secundária de adenomas do cólon pela American College of Gastroenterology.
Estudos do efeito do uso dos produtos lácteos na prevenção do câncer colorretal são controversos. Acredita-se que produtos lácteos protejam contra o câncer colorretal devido ao seu alto teor de cálcio; no entanto, alguns produtos lácteos, como queijo e creme, têm alto teor de gordura, o que pode contrabalançar o efeito protetor, possivelmente afetando a composição do ácido biliar no cólon. - Vitamina D
A vitamina D e seus metabólitos atuam como inibidores da progressão do câncer colorretal. Estudos de longo prazo revelaram uma ligação entre o baixo nível de vitamina D e o risco de muitos tipos de câncer, incluindo e principalmente o câncer colorretal. Não se sabe se o risco elevado de câncer colorretal, observado nos pacientes com deficiência de vitamina D, pode ser superado com a sua suplementação.
- Alho
O consumo de alho tem sido associado a um risco reduzido de adenomas do cólon em alguns estudos observacionais de pacientes com câncer colorretal. O alho foi incluído como um provável fator de proteção pelo Fundo Mundial para Pesquisa do Câncer/Instituto Americano de Pesquisa do Câncer.
- Consumo de peixe
O consumo de ácidos graxos ômega 3 (principalmente o óleo de peixe) tem sido associado a uma redução da frequência do câncer colorretal em estudos observacionais. Mas, a associação parece ser modesta e ensaios de intervenção ainda não foram relatados.
- Consumo de café
Estudos observacionais encontraram evidências conflitantes sobre a relação entre o consumo de café e o risco de câncer colorretal.
- Aspirina e AINEs (antiinflamatórias não esteroides)
Estudos demonstraram efeitos preventivos modestos a moderados em populações de risco médio e alto para o câncer colorretal. O uso regular de aspirina e outros AINEs está associado a uma redução de 20% a 40% no risco de adenomas e câncer colorretal em indivíduos com risco médio. Existem relatos de reduções de 50% na frequência do câncer colorretal após cinco anos de uso.
Várias questões-chave permanecem a serem estudadas:
- Como a aspirina ou AINEs podem proteger contra o câncer colorretal não é bem compreendida;
- A dose mínima e a duração para atingir o efeito protetor ainda são incertas na síndrome de Lynch;
- Finalmente, se os AINEs são benéficos para a prevenção em todos os subgrupos de pacientes, não está claro.
A acumulação de dados, tanto no contexto da prevenção primária como da prevenção secundária após o diagnóstico de câncer colorretal, sugere que o benefício dos AINEs pode estar limitado a determinados grupos clínicos ou subtipos moleculares de câncer colorretal.
- Terapia hormonal em mulheres
A terapia hormonal pós-menopausa (estrogênio combinado com progesterona e estrogênio isolado) tem sido associada a um risco reduzido de câncer colorretal, embora os dados sejam mais consistentes para o uso combinado. Um achado importante foi que, embora as mulheres que receberam estrogênio combinado com progesterona tivessem uma menor taxa de diagnóstico de câncer colorretal do que o grupo controle, os tumores que ocorreram nesse grupo foram encontrados em um estágio mais avançado do que aqueles encontrados no grupo controle.
Esses dados sugerem a possibilidade intrigante de que a terapia hormonal possa diminuir a incidência de terapia hormonal, mas não a mortalidade.
Mesmo antes dos dados mais recentes citados acima, a terapia hormonal pós-menopausa não foi recomendada para quimio-prevenção do câncer de cólon em mulheres, devido aos riscos de longo prazo associados à terapia. - Estatinas
Alguns dados observacionais sugerem que as estatinas estão associadas a um efeito protetor contra vários tipos de câncer, incluindo o câncer colorretal, mas, no geral, os dados são conflitantes. Uma redução modesta na incidência de câncer de cólon, como um ponto final secundário, foi observada em dois grandes estudos clínicos avaliando o benefício para doença arterial coronariana.
- Antioxidantes
Vários ensaios intervencionais avaliaram a eficácia dos antioxidantes na prevenção de adenomas colorretais. Ensaios clínicos controlados não encontraram evidências convincentes.
Quadro Clínico

Mesmo que a maioria dos casos seja assintomática no estágio inicial, alguns sintomas indicam que algo não vai bem e merecem ser investigados, pois podem, inclusive, estar relacionados a alguma outra doença do trato gastrointestinal. São eles:
- Diarreia por mais de uma semana ou má consistência das fezes por mais de três semanas
- Constipação
- Sangue visível nas fezes
- Inchaço abdominal
- Perda de peso sem motivo aparente
- Cansaço e fadiga constantes
Dependem localização e extensão do tumor e podem se manifestar 5 anos após o crescimento lento do câncer.
Pode ocorrer anemia, abdome agudo obstrutivo ou perfurativo, perda de peso, astenia leve, mudança do habito intestinal.
O cólon direito tem mais tendência a diarreia e o cólon esquerdo e sigmoide tem mais obstipação alternado com o numero de evacuações . No reto tem afilamento das fezes, muco serosanguinolento com dor ao evacuar.
Nos casos mais avançados se nota emagrecimento, palidez cutânea, icterícia por metástases hepáticas, palpação dos colons.
O toque retal pode detectar massa endurecida ou alteração na parede retal.
Diagnostico
História clínica e exame físico são essenciais. Laboratorialmente poderá mostra anemia ferropriva, alteração enzimas hepáticas , CEA será detectado em 65% dos pacientes mas pode se elevar em pancreatites, ulceras perfuradas, cirrose hepática, tabagistas e etc.
A certeza é feito pela colonoscopia com biopsia e tipo histopatológico e outras lesões em outras regiões.
A Pesquisa de DNA fecal ao contrário do teste de imunoquímica fecal (FIT) ou teste imunoquímico de sangue oculto nas fezes (FOBT), não procura sangue nas fezes, mas alterações genéticas específicas em células de pólipos ou cancro.
Ao longo do tempo, as células do cólon são libertadas para o lúmen intestinal (por esfoliação) e deste para as fezes.
A recolha destas células (e do seu DNA) é favorecida pela proliferação intensa das células do tumor. A resistência que têm à morte programada (apoptose), também permite que o DNA nas fezes se mantenha intacto.
As amostras são mantidas no frio (em gelo no transporte), e devem ser analisadas até 24 horas depois de serem colhidas.
O “alvo” do teste de DNA fecal são alterações genéticas comuns em cancros colorretais.
Sabe-se que a maior parte dos cancros colorretais resultam de alterações genéticas em células normais da mucosa intestinal, que podem então ser pesquisadas no DNA fecal - ex. alterações nos genes Kras, p53 e APC.
Usando este teste, pode também ser avaliada a instabilidade de microsatélites (MSI) - regiões que ficam tipicamente instáveis quando genes como MLH1, MSH2 e MSH6 (que participam na reparação do DNA) não funcionam correctamente.
O teste de DNA fecal, apesar de não invasivo, é um teste bastante dispendioso. Como noutros exames, se for positivo será necessário realizar uma colonoscopia.
Estadiamento
Determinar a extensão da lesão, acometimento de órgãos adjacentes como linfonodos peri tumorais, metástases a distância como Rx de tórax, tomografias, RNM e ultrassonografias endoscópica. A peça cirúrgica é de suma importância para a conduta.


Tratamento
A cirurgia é o tratamento primário para os 80% dos cânceres colorretais que não apresentam metástase. Apesar da cirurgia curativa e do uso de quimioterapia adjuvante moderna e/ou radioterapia (RT), mais de 40% dos pacientes que apresentam doença em estágio II ou III terão recorrência da doença após a terapia primária.
O tratamento de eleição nos casos A e B1 são cirúrgicos, nos casos mais avançados a partir B2 ou C devera ser submetido a QT , casos de reto baixo RDT associado a QT.
A cirurgia depende da localização e extensão do tumor. Deve ser retirado o tumor primário acompanhado de linfadenectomia regional com colectomias D ou E ou transverso.

As metástases hepáticas aparecem em 35% dos casos. A ressecção hepática aumenta a chance de cura nesses pacientes com melhores prognósticos em tumores pequenos e únicos. Pode ser realizado ablação nesses tumores.
Importante destacar que nos tumores de reto a RDT e QT pré operatória oferecem maior índice de ressecabilidade e preservação do esfíncter anal, nos tumores localmente avançados.
As cirurgias podem ser realizadas de forma laparotômica ou minimamente invasivas como as robóticas e laparoscópicas.
Biológicos e terapia alvo
O câncer colorretal é a quarta neoplasia mais freqüente entre os homens e a terceira entre as mulheres, acometendo aproximadamente um milhão de pessoas a cada ano no mundo.
Apesar da maioria dos pacientes detectar precocemente a neoplasia, com possibilidade de tratamento cirúrgico curativo, cerca de 20% dos pacientes apresentam doença a distância no momento do diagnóstico. Dentre aqueles submetidos ao tratamento local e adjuvante, 20% a 40% apresentarão recidivas sistêmicas durante o acompanhamento clínico. Quando os pacientes apresentam doença a distância, exceto em alguns casos de doença metastática exclusivamente hepática, o tratamento paliativo é indicado para o aumento da sobrevida e ganho na qualidade de vida.
A ressecção curativa de lesões hepáticas pode ser alcançada em pacientes com doença inicialmente ressecável, e em até 16% dos pacientes com doença inicialmente irressecável, devido às novas estratégias que possibilitam a cirurgia de conversão. A última década foi marcada por avanços na disponibilidade de novos fármacos com mecanismos de ação distintos e com impacto positivo no tratamento sequencial do câncer colorretal. Com a incorporação dessas novas estratégias, a sobrevida mediana dos pacientes com doença metastática praticamente dobrou ao longo dos últimos 10 anos, e parte dessa mudança se deve à introdução dos anticorpos monoclonais, capazes de inibir diferentes mecanismos de proliferação tumoral.
Os anticorpos monoclonais podem ser quiméricos, humanizados ou humanos. Os anticorpos quiméricos são formados por sequências de aminoácidos de origem humana, com sequências de origem murina nas regiões que se ligam aos epítopos antigênicos. No anticorpos humanizados, grande parte das sequências de aminoácidos é de origem humana, com parcela inferior a 5% correspondendo a origem murina. Os anticorpos humanos possuem sequências de origem 100% humana. À medida que se caminha para melhor compreensão do uso destes medicamentos na prática clínica, observa-se a necessidade de identificar biomarcadores relacionados ao prognóstico e predição de benefício.
A introdução do bevacizumabe representou um marco no tratamento do câncer colorretal. O bevacizumabe aumenta significativamente a eficácia da quimioterapia, e seu efeito ainda não foi relacionado à presença de biomarcadores. Os anticorpos anti-EGFR, por sua vez, também são medicamentos valiosos no tratamento do câncer colorretal metastático, muito embora seu benefício pareça estar limitado aos casos em que não há mutações do gene Kras.
Kras é abreviação do gene homologo do oncogênese viral do sarcoma de rato Kirsten. É um dos genes envolvidos em via chamada via receptor do fator de crescimento epidérmico (EGFR) e o teste avalia mutações ativadoras nos exons 2,3 e 4 do gene Kras (códons 12,13,59, 61, 117 e 146) para determinar terapias anti EGFR.
Vários genes que codificam proteínas chave na cascata de sinalização de EGFR encontram-se mutados em cânceres como o de colorretal e de pulmão e, em particular, mutações ativadoras do gene KRAS. A maioria destas mutações ocorrem nos códons 12 e 13 do exon 2, mas ocasionalmente nos exons 3 e 4. Foi observado que mutações nos códons 12, 13, 59, 61, 117 e 146 nos principais genes da família de oncogenes RAS resultam na elevação dos níveis da proteína ativada RAS-GTP, sendo considerada como biomarcador preditivo de resposta negativa a terapia com anticorpos anti-EGFR.
A FDA aprovou tratamento para pacientes com adenocarcinoma colorretal, com teste de Kras prévio. Portanto, as pesquisas de mutações nos genes KRAS e NRAS são imprescindíveis para o médico realizar a escolha do tratamento e, assim, aumentar a sobrevida nos pacientes.
A imunoterapia estimula o sistema imunológico a reconhecer e destruir células cancerígenas de forma mais eficaz e usadas em formas de câncer colorretal avançado (tumor não pode ser removido cirurgicamente, recidivou após o tratamento, doença está disseminada).
As células cancerigenas usam pontos de controle imunológicos para evitar de serem atacadas e os imunoterapicos tem como alvo esses pontos e restauram a resposta imunológica contra o câncer.
As células cancerígenas colorretais tem que ser testadas para alterações genéticas especificas com alto nível de instabilidade de microsatelites (MSI-H) ou genes de reparo de incompatibilidade de microssatélites (MSI-H) ou em genes e reparação de reparo de incompatilibidade de microssatélites (MMR).
Inibidores da PD-1 (pembrolizumabe e nivolumabe) tem como alvo a PD-1 , proteína do sistema imunológico (células T) e CTLA-4 que estimula resposta imunológica bloqueando a CTLA-4 outra proteína das células T que ajuda a mante las sob controle.
A terapia alvo usa drogas para identificar e atacar células cancerígenas com pouco dano as normais , agindo de modos diferentes atuando como ela cresce , se multiplica, auto repara ou interage com outras células.
- fator de crescimento endotelial vascular (VEGF)
Ele atua na proteina que ajuda os tumores a formarem novos vasos sanguíneos para obter nutrientes na angiogenese
- receptor do fator de crescimento epidérmico (EGFR)
Ele atua na proteina em quantidades elevadas na superfície das células cancerígenas fazendo o crescimento destas.
Quando ocorre a mutação no gene KRAS, NRAS ou BRAF esses medicamentos são ineficazes, portanto naqueles que não tem a mutação. Exceção quando cetuximabe é combinado com encorafenide aumenta a sobrevida
- alvo no gene BRAF
Menos de 10% dos canceres colorretais tem alteração neste que produz uma proteína BRAF anormal que os ajuda a crescer sendo usado encorafenibe que ataca a proteína .Administrado com cetuximabe reduz ou retarda crescimento colorretal avançado.
- outros
Regorafenibe que inibe as quinases que são proteínas da superfície ou próximas da superfície da célula que transmitem sinais importantes para o centro de controle da célula
Acompanhamento pós-operatório
Seguir as recorrências pois são assintomáticas , 80% ocorrem nos 2 primeiros anos e menos de 1% após 5 anos.
Importante exames de imagem, sanguíneos, marcadores tumorais e endoscópicas.
Programas de rastreamento do Câncer Colorretal - Prevenção
São políticas e planos de ação que cubram o programa de prevenção primária (prevenção da ocorrência), quanto secundária (diagnóstico precoce) e terciária (prevenção de deformidades, recidivas e morte). Portanto, ser submetido ao rastreamento do câncer colorretal é quando se é examinado quando está tudo bem, isto é, sem sinais e/ou sintomas.
O rastreamento regular do câncer colorretal é extremamente importante na prevenção da doença. A partir do momento que as primeiras células anormais começam a formar pólipos, até se tornar um câncer colorretal normalmente leva de 10-15 anos.
O rastreamento regular pode, em muitos casos, prevenir completamente o câncer colorretal, porque a maioria dos pólipos encontrados são removidos antes que tenham a chance de se transformar em câncer. O rastreamento também pode diagnosticar o câncer colorretal em estágio inicial (estágio I), quando é altamente curável (cerca de 95%).
Por fim, o rastreamento se resume ao conjunto de medidas tomadas para a identificação e retirada dos pólipos neoplásicos e da detecção do câncer precoce em indivíduos sem sinais e/ou sintomas.
Programas intensivos de vigilância pós-operatória são justificados, na esperança de que a detecção precoce de recorrências assintomáticas, aumente a proporção de pacientes potencialmente elegíveis para uma segunda terapia curativa.




